İzomorfizma, bir mineralin kristal yapısının, başka bir mineralin kristal yapısına benzemesidir. Bu benzerlik, minerallerin kimyasal bileşimleri ve kristal yapıları arasındaki benzerlikten kaynaklanır. İzomorfizma, jeolojide önemli bir kavramdır. Minerallerin izomorfizm yoluyla birbirleriyle nasıl etkileşime girdiğini anlamak, jeolojik süreçleri ve kayaç oluşumunu anlamamıza yardımcı olur.
İzomorfizma Türleri
İzomorfizma, iki mineral arasındaki benzerlik derecesine göre farklı türlere ayrılır:
Tam izomorfizma
Tam izomorfizm, iki mineralin kristal yapılarının tamamen aynı olduğu bir izomorfizm türüdür. Bu nedenle, bu mineraller birbiriyle tamamen çözünür. Tam izomorfizm, atom boyutları ve elektronegatiflikleri birbirine çok yakın olan mineraller arasında meydana gelir. Bu, atomların aynı kristal yapılarında aynı şekilde birbirleriyle etkileşime girmesine izin verir.
Tam izomorfizm gösteren bazı mineral örnekleri şunlardır:
- Kalsiyum karbonat (CaCO3) ve magnezyum karbonat (MgCO3)
- Sodyum klorit (NaCl) ve lityum klorit (LiCl)
- Alüminyum sülfat (Al2(SO4)3) ve demir sülfat (Fe2(SO4)3)
Yarı izomorfizma
Yarı izomorfizm, iki mineralin kristal yapılarının benzer olduğu, ancak bazı farklılıklar olduğu bir izomorfizm türüdür. Bu nedenle, bu mineraller birbiriyle kısmen çözünür. Yarı izomorfizm, atom boyutları ve elektronegatiflikleri birbirine biraz benzer olan mineraller arasında meydana gelir. Bu, atomların aynı kristal yapılarında benzer, ancak tam olarak aynı şekilde birbirleriyle etkileşime girmesine izin verir.
Yarı izomorfizm gösteren bazı mineral örnekleri şunlardır:
- Piroksen mineralleri (Mg, Fe, Ca)SiO3)
- Amfibol mineralleri (Ca, Na, K)2(Mg, Fe, Al)5Si8O22(OH, F, Cl)
- Feldspat mineralleri (Na, K)AlSi3O8
Pseudomorfizma
Pseudomorfizm, bir mineralin kristal yapısının, başka bir mineralin kristal yapısına benzemesidir. Bu, bir mineralin başka bir mineral tarafından yer değiştirmesiyle gerçekleşir.
Pseudomorfizm, iki mineral arasındaki kimyasal bileşim ve kristal yapı arasındaki farklılıktan kaynaklanır. Bir mineral, bir başka mineral tarafından yer değiştirdiğinde, yer değiştiren mineral, yer değiştiren mineralin kristal yapısına uyum sağlamak için kendi kristal yapısını değiştirebilir.
Pseudomorfizm gösteren bazı mineral örnekleri şunlardır:
- Kalsiyum karbonat (CaCO3) içeren bir kayaç, su ve karbondioksit ile etkileşime girdiğinde, kalsiyum karbonat, kalsiyum silikat (CaSiO3) ile yer değiştirebilir. Bu durumda, kalsiyum silikat kristalleri, kalsiyum karbonat kristallerinin şeklini alır.
- Bir kayaç, asit yağmurları ile etkileşime girdiğinde, kalsiyum karbonat (CaCO3), kalsiyum fosfat (Ca3(PO4)2) ile yer değiştirebilir. Bu durumda, kalsiyum fosfat kristalleri, kalsiyum karbonat kristallerinin şeklini alır.
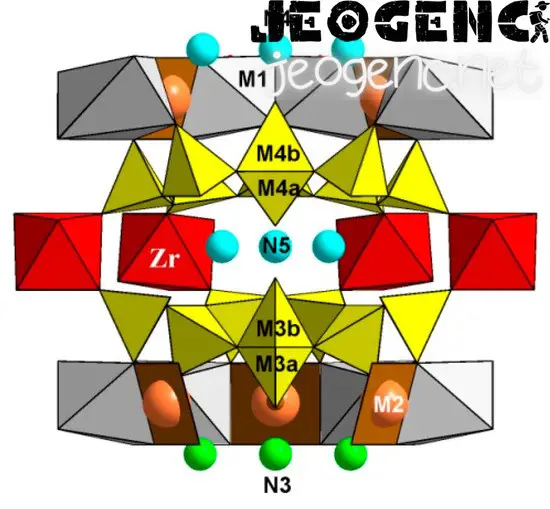
İzomorfizm Mekanizması
İzomorfizm, iki mineral arasındaki kimyasal bağların benzerliğinden kaynaklanır. Bu benzerlik, iki mineralin atomlarının boyutları ve elektronegatiflikleri arasındaki benzerlikten kaynaklanır. Atomlar arasındaki kimyasal bağların gücü, atomların boyutları ve elektronegatiflikleri arasındaki ilişkiye bağlıdır. Atomlar arasındaki elektronegatiflik farkı ne kadar büyükse, kimyasal bağ o kadar zayıf olur.
İzomorfizm gösteren mineraller arasındaki atomların boyutları ve elektronegatiflikleri birbirine yakındır. Bu nedenle, bu mineraller arasındaki kimyasal bağlar güçlüdür. Bu, bu minerallerin birbiriyle çözünürlüğünü ve yer değiştirmelerini kolaylaştırır.
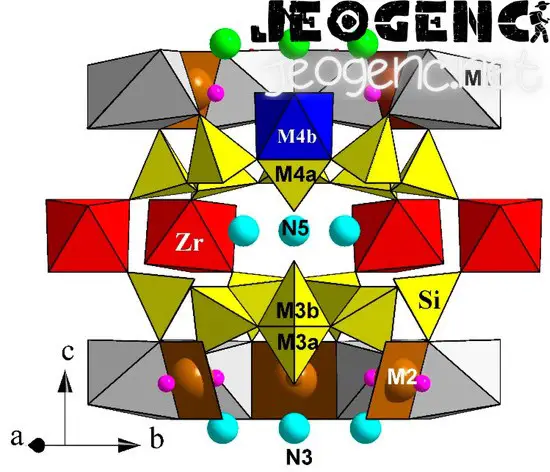
İzomorflukla İlgili Bazı Kurallar (Krauskopf, 1989)
İki bileşik tamamen aynı ya da çok benzer kristal şekline sahipse bunlar izomorfturlar.
Bu kural, iki bileşikteki atomların kristal yapıda aynı veya benzer şekilde birbirleriyle etkileşime girmesine izin verir. Bu, iki bileşiğin aynı veya benzer fiziksel özelliklere sahip olmasına neden olur.
Örnek: Kalsiyum karbonat (CaCO3) ve magnezyum karbonat (MgCO3) tam izomorfizm gösterir. Bu bileşiklerin her ikisi de aynı kristal yapıya sahiptir (triklin). Bu, her iki bileşiğin de aynı fiziksel özelliklere sahip olmasına neden olur, yani aynı sertlik, yoğunluk ve erime noktasına sahiptirler.
İzomorf iki bileşik, iyon yarıçapları birbirinin aynı ya da çok benzer iyonlar içermelidir.
Bu kural, iki bileşiğin atomlarının kristal yapının aynı boşluklarında oturmasına izin verir. Bu, iki bileşiğin aynı veya benzer kimyasal özelliklere sahip olmasına neden olur.
Örnek: Sodyum klorit (NaCl) ve lityum klorit (LiCl) tam izomorfizm gösterir. Bu bileşiklerin her ikisinde de aynı iyon yarıçapı vardır (0,181 nm). Bu, her iki bileşiğin de aynı kimyasal özelliklere sahip olmasına neden olur, yani aynı çözünürlüğe ve elektrik iletkenliğine sahiptirler.
İzomorf iki bileşik katı ergiyik serisi oluşturabilir. Yani iki uç ürünü farklı oranlarda içeren homojen kristaller oluşturabilir.
İki bileşiğin atomlarının kristal yapıda aynı veya benzer şekilde birbirleriyle etkileşime girmesine izin verir. Bu, iki bileşiğin farklı oranlarda karıştırılabilmesini sağlar.
Örnek: Kalsiyum karbonat (CaCO3) ve magnezyum karbonat (MgCO3) tam izomorfizm gösterir. Bu bileşikler, farklı oranlarda karıştırılarak katı ergiyik serisi oluşturabilir. Örneğin, 100 gram kalsiyum karbonat ve 50 gram magnezyum karbonat karıştırıldığında, 150 gram katı ergiyik elde edilir. Bu katı ergiyik, %66,6 kalsiyum karbonat ve %33,3 magnezyum karbonat içerir.
İzomorfluğun en iyi ve katı ergiyiğin en mükemmel geliştiği bileşikler, iyonları benzer kovalent karakter gösteren bileşiklerdir. Örneğin Zn+2 ve Fe+2 birbirine çok yakın büyüklükte olmalarına rağmen, sfaleritin yapısı pirotinin yapısından farklıdır. Çünkü Zn-S bağı Fe-S bağına göre daha kovalenttir. Bu nedenle sfalerit ve pirotin arasında ancak çok sınırlı bir şekilde katı ergiyik gelişebilir.
Bu kural, iki bileşiğin atomlarının kristal yapıda aynı veya benzer şekilde birbirleriyle etkileşime girmesine izin verir. İki bileşiğin arasında güçlü bağlar oluşmasına neden olur.
Örnek: ZnS (sfalerit) ve FeS (pirotin) mineralleri, Zn+2 ve Fe+2 iyonları arasındaki benzer iyon yarıçapları nedeniyle izomorfizm gösterir. Ancak, Zn-S ve Fe-S bağları arasındaki kovalent karakter farkı nedeniyle, bu mineraller arasında katı ergiyik serisi çok sınırlı bir şekilde gelişebilir.
